АВТОРСКА СПРАВКА ЗА ПРИНОСНИЯ ХАРАКТЕР НА ТРУДОВЕТЕ на гл. ас. д-р Валя Кирилова Николова Катедра Фармацевтична и приложна органична химия, Факултет п
|
|
|
- Росица Даскалова
- преди 4 години
- Прегледи:
Препис
1 АВТОРСКА СПРАВКА ЗА ПРИНОСНИЯ ХАРАКТЕР НА ТРУДОВЕТЕ на гл. ас. д-р Валя Кирилова Николова Катедра Фармацевтична и приложна органична химия, Факултет по химия и фармация, СУ "Св. Климент Охридски", за участие в конкурс за "Доцент" по професионално направление 4.2. Химически науки (Теоретична химия), обявен в ДВ, бр. 50 от г. Авторската справка е направена върху 20 научни публикации на кандидата, от които 19 са в реферирани и индексирани списания с общ импакт фактор (IF) , 1 е в рефериранo списаниe без импакт фактор. Пет от публикациите [1-5] са използвани за придобиване на образователната и научна степен "доктор". Включването им в настоящата справка се обосновава от продължаването на изследванията в съответната тематика и след защита на дисертационния труд. Към момента на подаване на документите са забелязани общо 210 цитата (189 по Scopus), h-индексът на кандидата е 7. Част от получените резултати са включени в 6 дипломни работи и са представени на 6 международни и национални конференции. Представените трудове са в областта на теоретичната химия. Една част от научната работа е свързана с изследване на приложението на атомния електростатичен потенциал (АЕП) като индекс на реактивоспособност a друга част с изследване на факторите, контролиращи процесите на комплексообразуване на циклодекстрини с метални йони. Научните приноси на кандидата могат да се групират тематично в четири основни направления: I. Приложение на АЕП като индекс, описващ реактивоспособността на молекулите при процесите на водородно и π-водородно свързване [1, 2, 3, 9, 10, 13, 14, 19]. II. Изследване на приложението на АЕП при химични реакции и при анализиране на природата на ефектите на заместителите в ароматни системи [4, 5, 6, 7, 8]. III. Изясняване на факторите, управляващи процесите на комплексообразуване на циклодекстрини и метални йони [15, 16, 17, 18]. IV. Моделиране на процеси на конкуренция между различни метални йони в биологични системи [11, 12, 20]. Номерацията на публикациите съответства на списъка с научни трудове на кандидата
2 I. Приложение на АЕП като индекс, описващ реактивоспособността на молекулите при процесите на водородно и π-водородно свързване [1, 2, 3, 9, 10, 13, 14, 19]. 1. Изследвано е приложението на АЕП като дескриптор, описващ реактивоспособността на молекулите при процеса на водородно свързване на различни серии протонакцепторни молекули и амоняк като протондонор [1,2]. Получените резултати показват, че стойностите на АЕП могат успешно да се прилагат при охарактеризиране на протонодонорната способност на молекули, имащи различно обкръжение при водородния атом. В обзорна публикация [3] са разгледани три различни типа водородно свързани комплекси: (1) серии протонакцепторни молекули (R-CHO и R-CN) с HF като протон донор; (2) серии монозаместени и дизаместени ацетилени с амоняк като протондонор; (3) (HCN) n водородно свързани клъстери. От установените зависимости за всички изследвани серии може да се направи извод, че АЕП може да предсказва количествено способността на различни видове молекули да формират водородни връзки. 2. Установено е, че АЕП може да се използва и за описване на реактивоспособността на молекулите при процесите на π-водородно свързване. Изследвани са две серии π- водородно свързани комплекси: (1) серия заместени бензени и фенол и (2) серия заместени феноли и хексаметилбензен [9,14,19]. Резултатите показват, че изчислените енергии на взаимодействие корелират добре със стойностите на АЕП. При комплексите на феноли с хексаметилбензен, стойностите на атомния електростатичен потенциал описват добре и вътрешномолекулните фактори, свързани с ефектите на свръхспрежение на метиловите групи върху процеса на π-водородно свързване. 3. Получени са добри корелации между стойностите на електростатичния потенциал при атомите, участващи в образуването на водородна връзка между заместени аденини и тимин, което би могло да намери приложение при дизайна на нови биологично активни аденинови производни [10]. За да се анализира способността на отделните атомни центрове в 5 бази (нуклеотида), участващи в образуването на ДНК и РНК, е изследвана моделна серия от 64 молекули и е намерено, че най-добър дескриптор, характеризиращ способността за водородно свързване, е АЕП [13]. 2
3 II. Изследване на приложението на АЕП при химични реакции и при анализиране на природата на ефектите на заместителите в ароматни системи [4,5,6,7,8]. 1. При изследване на реакцията на протонен трансфер на серия заместени феноли с хидроксилен анион е установено, че АЕП е подходящ молекулен параметър, описващ добре тяхната реактивоспособност [4]. Реактивоспособността на бензилфлуориди към S N 2 обменната реакция с флуорен анион също се предсказва перфектно със стойностите на атомния електростатичен потенциал при въглеродните атоми в изходните реактанти и в преходните състояния [5]. 2. Друго приложение на АЕП, което бе изследвано, е неговото използване за охарактеризиране на ефектите на заместителите в ароматни системи [8]. Изследвана е серия от монозаместени на различна позиция бензени. От получените отлични линейни зависимости между стойностите на молекулния електростатичен потенциал (МЕП) в точки, разположени на различно разстояние над ароматното ядро и константите на заместителите е установено, че стойностите на МЕП отразяват добре и индукционните (through-bond и through-space) и резонансните ефекти. 3. Показано е, че АЕП е един е много подходящ електронен параметър (наред с атомни заряди като например NBO и Hirshfeld заряди), който успешно може да се използва при изучаване на природата на вътрешномолекулните взаимодействия [7]. Стойностите на АЕП могат да се използват и за описване на ефектите на полярни заместители върху интензитета на валентното трептене на С=О група [6]. За разлика от атомните заряди, АЕП е точно дефинирана квантово-механична величина, съответстваща на точността на използваната вълнова функция. 3
4 III. Изясняване на факторите, управляващи процесите на комплексообразуване на циклодекстрини и метални йони [15, 16, 17, 18]. 1. При моделиране на процесите на комплексообразуване на α- и β- циклодекстрини с метални йони от IIA/IIB група е установено, че поради концентриране на отрицателния заряд в равнината на тесния ръб на циклодекстрините, там е най-благоприятната позиция за свързване на металния йон [15,16]. За всяка една от изследваните групи (IIА/IIB) колкото по-малък е йонният радиус, толкова термодинамично по-изгодно е образуването на комплекс с α- и β-циклодекстрин. И при двата вида циклодекстрини отчитането на водата като разтворител прави комплексообразуването термодинамично по-неизгодно. 2. При изследване на комплексите на трите типа представители на циклодекстрините (α-, β- и γ-цд) с метални йони от IA, IIA и IIIA групи е показано, че въпреки че трите циклодекстрина се различават по размера на кухината, те проявяват сходен афинитет. Най-голям е афинитетът към метални йони с по-малък йонен радиус и по-голям заряд [17]. Увеличаването на полярността на средата води до увеличаване на стойносттта на свободната енергия на реакцията и тя става термодинамично по-неизгодна в сравнение с реакцията в газова фаза. Молекулата на циклодекстрина притежава голяма гъвкавост, което дава възможност на металния йон да намери своята оптимална позиция в равнината на тесния ръб на циклодекстрина. Металните йони с по-голям заряд причиняват по-големи деформации на молекулата на циклодекстрина. 3. При изясняване на факторите, контролиращи процеса на хидратиране на наймалкият представител от семейството на циклодекстрините - α-циклодекстрин, е установено, че първата молекула вода се свързва отново в равнината на тесния ръб, където е концентрирана електронна плътност, което улеснява взаимодействието с молекулата на водата. Първата молекула вода има решаваща роля за процеса на хидратиране на циклодекстрина, тя служи като котва, с която се свързват с водородни връзки следващите постъпващи в кухината водни молекули. Показано е, че броят на действителните молекули вода, разположени в кухината на α-cd, не може да бъде по-голям от 6. Причината за стабилността на водните клъстери в кухината на циклодекстрина се дължи на образуването на мрежа от водородни връзки, както между съседни водни молекули, така и между водните молекули и циклодекстрина. 4
5 IV. Моделиране на процеси на конкуренция между различни метални йони в биологични системи [11, 12, 20]. 1. Чрез квантовохимични изчисления е моделирана реакцията на заместване на Fe 3+ с Ga 3+ в комплекс, имитиращ активния център на редуцираната форма на ензима рибонуклеотид редуктаза (ключов ензим в процеса на растеж на туморните клетки), и е установено, че Ga 3+ може да измести Fe 3+, което може да доведе до инхибирането на този ензим [11]. Друг моделиран процес е процесът на конкуренция между Fe 3+ и Ga 3+ с лиганди, имитиращи центъра на свързване на трансферина. Поради близките свойства, които двата йона притежават, комплексите на свързване са подобни, но от изчислените стойности на свободната Гибсова енергия може да се направи извод, че термодинамично по-изгодна е реакцията на свързване на Fe 3+ с трансферин. 2. При изследването на механизма на конкуренция на Fe 2+ - М 2+ (М = Mg, Mn, Zn) в протеини, където желязото не е свързано в хем група, е установено, че факторите, контролиращи процеса са три: физикохимичните свойства на металните катиони; свойствата на центровете на свързване на протеина и свободната цитозолна концентрация на конкуриращите се метални катиони [12]. При процесите на конкуренция на Fe 2+ / Мg 2+ и Fe 2+ / Мn 2+, Fe 2+ не може да бъде изместено от двата метала, но при конкуренцията с по-силния преходен метал Zn 2+, резултатите показват, че протеинът има по-голям афинитет към Zn 2+, отколкото към Fe 2+. Ключов фактор за металната конкуренция тук е относителната концентрация на катионите в клетката. 3. Изследвано е взаймодействието между лактоза (млечна захар, съдържаща се в млякото и повечето млечни продукти) и Ca 2+, Mg 2+ и Zn 2+ йони, които често присъстват като добавки към млякото [20]. Изчисленията показват, че и трите метални катиона могат успешно да се свържат с лактозата, като процесът на конкуренция между тях зависи от физикохимичните свойства на съответния катион и от диелектричните свойства на средата. Реакцията е термодинамично по-изгодна, когато протича с метални йони с по-малък йонен радиус, като Mg 2+ и Zn 2+. 5
РЕЦЕНЗИЯ
 Р Е Ц Е Н З И Я по конкурса за доцент в професионално направление 4.2 Химически науки (Теоретична химия) обявен в Държавен вестник, бр. 50 от 15. 06. 2018 г. от проф. д-р Анела Николова Иванова, СУ Св.
Р Е Ц Е Н З И Я по конкурса за доцент в професионално направление 4.2 Химически науки (Теоретична химия) обявен в Държавен вестник, бр. 50 от 15. 06. 2018 г. от проф. д-р Анела Николова Иванова, СУ Св.
21_Авторска справка за приносния характер на трудовете
 АВТОРСКА СПРАВКА ЗА ПРИНОСНИЯ ХАРАКТЕР НА ТРУДОВЕТЕ на гл. ас. д-р Йорданка Борисова Иванова Катедра Патология на растенията и химия Факултет по Екология и ландшафтна архитектура, Лесотехнически университет
АВТОРСКА СПРАВКА ЗА ПРИНОСНИЯ ХАРАКТЕР НА ТРУДОВЕТЕ на гл. ас. д-р Йорданка Борисова Иванова Катедра Патология на растенията и химия Факултет по Екология и ландшафтна архитектура, Лесотехнически университет
Справка за приносния характер на трудовете на гл. ас. д-р Диана Чешмеджиева Катедра Фармацевтична и приложна органична химия, Факултет по химия и фарм
 Справка за приносния характер на трудовете на гл. ас. д-р Диана Чешмеджиева Катедра Фармацевтична и приложна органична химия, Факултет по химия и фармация, СУ Св. Климент Охридски, за участие в конкурс
Справка за приносния характер на трудовете на гл. ас. д-р Диана Чешмеджиева Катедра Фармацевтична и приложна органична химия, Факултет по химия и фармация, СУ Св. Климент Охридски, за участие в конкурс
Справка за приносния характера на трудовете на д-р Стоян Иванов Гуцов
 Авторска справка за приносния характера на трудовете на доц. д-р Стоян Иванов Гуцов Изследванията на доц. д-р Стоян Иванов Гуцов са концентрирани в следните научни направления: I. Получаване и охарактеризиране
Авторска справка за приносния характера на трудовете на доц. д-р Стоян Иванов Гуцов Изследванията на доц. д-р Стоян Иванов Гуцов са концентрирани в следните научни направления: I. Получаване и охарактеризиране
РЕЦЕНЗИЯ от доц. д-р Галя Костова Маджарова Член на научното жури по конкурса за доцент по направление 4.2. Химически науки (Теоретична химия) към Кат
 РЕЦЕНЗИЯ от доц. д-р Галя Костова Маджарова Член на научното жури по конкурса за доцент по направление 4.2. Химически науки (Теоретична химия) към Катедра Органична химия и фармакогнозия при Факултета
РЕЦЕНЗИЯ от доц. д-р Галя Костова Маджарова Член на научното жури по конкурса за доцент по направление 4.2. Химически науки (Теоретична химия) към Катедра Органична химия и фармакогнозия при Факултета
Microsoft Word - Recenzia-Kapralov.doc
 СТАНОВИЩЕ по конкурс за заемане на академичната длъжност Доцент по професионално направление Химически науки, шифър 4.2. (Органична и органометална химия) обявен в Държавен вестник, бр. 44/29.05.2018 г.
СТАНОВИЩЕ по конкурс за заемане на академичната длъжност Доцент по професионално направление Химически науки, шифър 4.2. (Органична и органометална химия) обявен в Държавен вестник, бр. 44/29.05.2018 г.
Р Е Ц Е Н 3 И Я
 Р Е Ц Е Н 3 И Я По конкурс за академичното звание доцент, професионално направление 4.1. Физически науки, специалност Физика на кондензираната материя с кандидат: Радостина Стефанова Камбурова, доктор,
Р Е Ц Е Н 3 И Я По конкурс за академичното звание доцент, професионално направление 4.1. Физически науки, специалност Физика на кондензираната материя с кандидат: Радостина Стефанова Камбурова, доктор,
Софийски университет Св. Климент Охридски Факултет по химия и фармация Катедра Органична химия и фармакогнозия Автореферат На дисертацията на на Искра
 Софийски университет Св. Климент Охридски Факултет по химия и фармация Катедра Органична химия и фармакогнозия Автореферат На дисертацията на на Искра Зарева Колева за присъждане на научната и образователна
Софийски университет Св. Климент Охридски Факултет по химия и фармация Катедра Органична химия и фармакогнозия Автореферат На дисертацията на на Искра Зарева Колева за присъждане на научната и образователна
Microsoft Word - Ahmedova_spravka.doc
 Авторска справка за приносите на научните трудове на д-р Анифе Исмаилова Ахмедова във връзка с участие в конкурс за доцент (професионално направление 4.2 Химически науки Аналитична химия, обявен в ДВ,
Авторска справка за приносите на научните трудове на д-р Анифе Исмаилова Ахмедова във връзка с участие в конкурс за доцент (професионално направление 4.2 Химически науки Аналитична химия, обявен в ДВ,
химия Използвайте следните стойности : ("L" означава литри) Универсална газова константа: R = 8, Ра.L1(к.mоl) = 8,31 J/(к.mоl) = 0,082 аtm.l1(к.
 химия Използвайте следните стойности : ("L" означава литри) Универсална газова константа: R = 8,31.103 Ра.L1(к.mоl) = 8,31 J/(к.mоl) = 0,082 аtm.l1(к.mоl) Число на Авогадро: N A = 6,0.1023 mol Стандартни
химия Използвайте следните стойности : ("L" означава литри) Универсална газова константа: R = 8,31.103 Ра.L1(к.mоl) = 8,31 J/(к.mоl) = 0,082 аtm.l1(к.mоl) Число на Авогадро: N A = 6,0.1023 mol Стандартни
УКАЗАНИЯ ЗА ПРОВЕРКА И ОЦЕНКА НА ПИСМЕНИТЕ КАНДИДАТ-СТУДЕНТСКИ РАБОТИ ПО ХИМИЯ ЗА УЧЕБНАТА 2014/2015 г В МУ-ПЛЕВЕН I. ОБЩИ ПОЛОЖЕНИЯ. Преглеждането и
 УКАЗАНИЯ ЗА ПРОВЕРКА И ОЦЕНКА НА ПИСМЕНИТЕ КАНДИДАТ-СТУДЕНТСКИ РАБОТИ ПО ХИМИЯ ЗА УЧЕБНАТА 2014/2015 г В МУ-ПЛЕВЕН I. ОБЩИ ПОЛОЖЕНИЯ. Преглеждането и оценяването на писмените работи се извършват в съответствие
УКАЗАНИЯ ЗА ПРОВЕРКА И ОЦЕНКА НА ПИСМЕНИТЕ КАНДИДАТ-СТУДЕНТСКИ РАБОТИ ПО ХИМИЯ ЗА УЧЕБНАТА 2014/2015 г В МУ-ПЛЕВЕН I. ОБЩИ ПОЛОЖЕНИЯ. Преглеждането и оценяването на писмените работи се извършват в съответствие
TEMA 3 Химична връзка Част 1.1. Химична връзка исторически аспекти на теорията Какво трябва да знам? определение за химична връзка; класическите предс
 TEMA 3 Химична връзка Част 1.1. Химична връзка исторически аспекти на теорията определение за химична връзка; класическите представи на Люис и Косел за причината за образуване на химична връзка Част 1.2.Ковалентна
TEMA 3 Химична връзка Част 1.1. Химична връзка исторически аспекти на теорията определение за химична връзка; класическите представи на Люис и Косел за причината за образуване на химична връзка Част 1.2.Ковалентна
О Т З И В
 Рецензия Върху дисертационния труд на асистент Кирилка Стефанова Младенова докторант към Катедра Биохимия, Биологически факултет, СУ Климент Охридски за присъждане на образователната и научна степен доктор
Рецензия Върху дисертационния труд на асистент Кирилка Стефанова Младенова докторант към Катедра Биохимия, Биологически факултет, СУ Климент Охридски за присъждане на образователната и научна степен доктор
IMH'I'AS'Lecture'ALL'UCII'r'19
 ИНСТРУМЕНТАЛНИ МЕТОДИ ЗА АНАЛИЗ АТОМНА СПЕКТРОХИМИЯ ЛЕКЦИЯ 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ СПЕКТРИ Химия ІІ курс редовно, летен семестър 2019 Pag Лекция 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ
ИНСТРУМЕНТАЛНИ МЕТОДИ ЗА АНАЛИЗ АТОМНА СПЕКТРОХИМИЯ ЛЕКЦИЯ 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ СПЕКТРИ Химия ІІ курс редовно, летен семестър 2019 Pag Лекция 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ
До Председателя на Научния съвет на ИЕ при БАН
 До Председателя на Факултетния съвет на Физическия факултет на СУ Кл. Охридски Р Е Ц Е Н З И Я от Проф. Кирил Борисов Благоев Относно: Конкурс за присъждане на научното звание доцент по професионалното
До Председателя на Факултетния съвет на Физическия факултет на СУ Кл. Охридски Р Е Ц Е Н З И Я от Проф. Кирил Борисов Благоев Относно: Конкурс за присъждане на научното звание доцент по професионалното
ПРОГРАМА за кандидат-студентския изпит по Химия за специалността Медицина Университет Проф. д-р А. Златаров -бургас 1. Строеж на атома. 2. Периодичен
 ПРОГРАМА за кандидат-студентския изпит по Химия за специалността Медицина Университет Проф. д-р А. Златаров -бургас 1. Строеж на атома. 2. Периодичен закон и периодична система на химичните елементи. 3.
ПРОГРАМА за кандидат-студентския изпит по Химия за специалността Медицина Университет Проф. д-р А. Златаров -бургас 1. Строеж на атома. 2. Периодичен закон и периодична система на химичните елементи. 3.
Р Е Ц Е Н З И Я от Снежана Георгиева Христева-Краева, д.м.н., професор, ПУ П.Хилендарски на материалите, представени за участие в конкурс за заемане н
 Р Е Ц Е Н З И Я от Снежана Георгиева Христева-Краева, д.м.н., професор, ПУ П.Хилендарски на материалите, представени за участие в конкурс за заемане на академичната длъжност доцент по професионално направление
Р Е Ц Е Н З И Я от Снежана Георгиева Христева-Краева, д.м.н., професор, ПУ П.Хилендарски на материалите, представени за участие в конкурс за заемане на академичната длъжност доцент по професионално направление
ХИМИЯ
 ХИМИЯ (2009) Националност Име Презиме Фамилия (Моля, напишете с печатни букви тритете си имена, като подчертаете фамилното си име) Оценки І Напишете номера на правилния отговор в съответната клетка за
ХИМИЯ (2009) Националност Име Презиме Фамилия (Моля, напишете с печатни букви тритете си имена, като подчертаете фамилното си име) Оценки І Напишете номера на правилния отговор в съответната клетка за
Microsoft Word - D.Todorovsky-Retsenziya-T. Todorov.doc
 РЕЦЕНЗИЯ на дисертационния труд на маг. Тихомир Радев Тодоров, редовен докторант към ИОНХ при БАН с научен ръководител доц. д-р Стефка Тепавичарова на тема «Форми на съществуване на преходни метали в повърхностни
РЕЦЕНЗИЯ на дисертационния труд на маг. Тихомир Радев Тодоров, редовен докторант към ИОНХ при БАН с научен ръководител доц. д-р Стефка Тепавичарова на тема «Форми на съществуване на преходни метали в повърхностни
Р Е Ц Е Н З И Я
 Р Е Ц Е Н З И Я от проф. д-р инж. Румен Дончев Недков, член на Научно жури съгласно Заповед РД38-26/22.04.2016 на Ректора на СУ Св.Кл.Охридски и Протокол No 1/27.0.2016 г от заседание на Научното жури
Р Е Ц Е Н З И Я от проф. д-р инж. Румен Дончев Недков, член на Научно жури съгласно Заповед РД38-26/22.04.2016 на Ректора на СУ Св.Кл.Охридски и Протокол No 1/27.0.2016 г от заседание на Научното жури
Лекция Приложение на линейната многопроменлива регресия за изчисляване на топлини на образуване на алкани Дефиниция на топлина на образуване Топлина н
 Лекция Приложение на линейната многопроменлива регресия за изчисляване на топлини на образуване на алкани Дефиниция на топлина на образуване Топлина на образуване на едно химично съединение се нарича енталпията
Лекция Приложение на линейната многопроменлива регресия за изчисляване на топлини на образуване на алкани Дефиниция на топлина на образуване Топлина на образуване на едно химично съединение се нарича енталпията
BULGARIAN PARTICIPATION IN THE SPS AND PS EXPERIMENTS
 Молекулно-динамични симулации в различни термодинамични ансамбли Каноничен ансамбъл като Ако малката система е състои от една частица Брой на клетките във фазовото пространство, където може да се намира
Молекулно-динамични симулации в различни термодинамични ансамбли Каноничен ансамбъл като Ако малката система е състои от една частица Брой на клетките във фазовото пространство, където може да се намира
Р Е Ц Е Н З И Я
 Р Е Ц Е Н З И Я на дисертационен труд, представен за придобиване на научната степен "доктор на науките по професионално направление 4.2. Химически науки (Органична химия) Автор на дисертацията: д-р Иво
Р Е Ц Е Н З И Я на дисертационен труд, представен за придобиване на научната степен "доктор на науките по професионално направление 4.2. Химически науки (Органична химия) Автор на дисертацията: д-р Иво
1 Термодинамика на идеалния газ: между молекулите няма взаимодействие. Изотермичното свиване нe води до промяна на вътрешната енергия. RT pv E E U R c
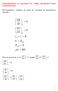 Термодинамика на идеалния газ: между молекулите няма взаимодействие. Изотермичното свиване нe води до промяна на вътрешната енергия. E E ot kin 0 0 0 Нека да докажем, че от 0 следва: 0, 0, 0 0 0 ) ( )
Термодинамика на идеалния газ: между молекулите няма взаимодействие. Изотермичното свиване нe води до промяна на вътрешната енергия. E E ot kin 0 0 0 Нека да докажем, че от 0 следва: 0, 0, 0 0 0 ) ( )
Авторска справка за приносите на научните трудове на гл. ас. д-р Станимир Стоянов Стоянов във връзка с участие в конкурс за доцент по професионално на
 Авторска справка за приносите на научните трудове на гл. ас. д-р Станимир Стоянов Стоянов във връзка с участие в конкурс за доцент по професионално направление 4.2. Химически науки (органична химия, органична
Авторска справка за приносите на научните трудове на гл. ас. д-р Станимир Стоянов Стоянов във връзка с участие в конкурс за доцент по професионално направление 4.2. Химически науки (органична химия, органична
Microsoft Word - recenzia Rumi Coneva ot A Momchilova.doc
 Р Е Ц Е Н З И Я по конкурс за доцент за нуждите на секция Електроиндуцирани и адхезивни свойства на ИБФБМИ- БАН. Рецензент: професор Албена Момчилова, дбн член на научно жури за избор на доцент съгласно
Р Е Ц Е Н З И Я по конкурс за доцент за нуждите на секция Електроиндуцирани и адхезивни свойства на ИБФБМИ- БАН. Рецензент: професор Албена Момчилова, дбн член на научно жури за избор на доцент съгласно
Приложение 3:
 ПРИЛОЖЕНИЕ 3 Минимални изисквания към научната и преподавателската дейност на кандидатите за придобиване на научна степен и за заемане на академичните длъжности "главен асистент", "доцент" и "професор"
ПРИЛОЖЕНИЕ 3 Минимални изисквания към научната и преподавателската дейност на кандидатите за придобиване на научна степен и за заемане на академичните длъжности "главен асистент", "доцент" и "професор"
Microsoft Word - Vas_25a.doc
 126 АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА 25. АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА Полярната група на АПАВ, която чрез дисоциирането си придава водоразтворимост на цялата молекула, може да бъде COONa, OSO3Na
126 АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА 25. АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА Полярната група на АПАВ, която чрез дисоциирането си придава водоразтворимост на цялата молекула, може да бъде COONa, OSO3Na
КАНДИДАТСТУДЕНТСКИ ИЗПИТ по Химия за специалностите "Медицина", "Дентална медицина" и "Фармация" г. Неорганична химия 1. Главното квантово
 КАНДИДАТСТУДЕНТСКИ ИЗПИТ по Химия за специалностите "Медицина", "Дентална медицина" и "Фармация" 08.07.2019 г. Неорганична химия 1. Главното квантово число n определя: a. енергията на електрона и размерите
КАНДИДАТСТУДЕНТСКИ ИЗПИТ по Химия за специалностите "Медицина", "Дентална медицина" и "Фармация" 08.07.2019 г. Неорганична химия 1. Главното квантово число n определя: a. енергията на електрона и размерите
Изпитни въпроси и задачи
 УКЗНИЯ За проверка и оценка на кандидат-студентските работи по Химия II - 13.6.15 г. за учебната 15/16 г. I. ОБЩИ ПОЛОЖЕНИЯ: Задачите са от материала по обща, неорганична и органична химия според учебниците
УКЗНИЯ За проверка и оценка на кандидат-студентските работи по Химия II - 13.6.15 г. за учебната 15/16 г. I. ОБЩИ ПОЛОЖЕНИЯ: Задачите са от материала по обща, неорганична и органична химия според учебниците
СТАНОВИЩЕ на доц. д-р Климент Минев Найденов, ръководител на Катедра Регионално развитие, ГГФ член на научно жури в конкурс за заемане на академичната
 СТАНОВИЩЕ на доц. д-р Климент Минев Найденов, ръководител на Катедра Регионално развитие, ГГФ член на научно жури в конкурс за заемане на академичната длъжност доцент в Област на висше образование 1. Педагогически
СТАНОВИЩЕ на доц. д-р Климент Минев Найденов, ръководител на Катедра Регионално развитие, ГГФ член на научно жури в конкурс за заемане на академичната длъжност доцент в Област на висше образование 1. Педагогически
Механизми за натрупване на СО 2 при водораслите. Ролята на RUBISCO. Фотореспирация. Типове транспортни протеини. Типове въглеродни анхидрази и клетъчн
 Механизми за натрупване на СО 2 при водораслите. Ролята на RUBISCO. Фотореспирация. Типове транспортни протеини. Типове въглеродни анхидрази и клетъчна локализация. Ролята на карбоксизомите и пиреноида.
Механизми за натрупване на СО 2 при водораслите. Ролята на RUBISCO. Фотореспирация. Типове транспортни протеини. Типове въглеродни анхидрази и клетъчна локализация. Ролята на карбоксизомите и пиреноида.
Microsoft Word - Vas_9.doc
 ДИРЕКТНИ БАГРИЛА 55 8. ДИРЕКТНИ БАГРИЛА Директните багрила са водоразтворими вещества, които във воден разтвор се дисоциират на багрилен анион и компенсиращ катион. Наричат се директни, тъй като багрилните
ДИРЕКТНИ БАГРИЛА 55 8. ДИРЕКТНИ БАГРИЛА Директните багрила са водоразтворими вещества, които във воден разтвор се дисоциират на багрилен анион и компенсиращ катион. Наричат се директни, тъй като багрилните
РЕЦЕНЗИЯ
 РЕЦЕНЗИЯ по конкурс за заемане на академична длъжност доцент по специалност 4.1 физически науки/квантова информатика/ обявен в ДВ бр.102 от 12.12.2014 г. с единствен кандидат Петър Александров Иванов,
РЕЦЕНЗИЯ по конкурс за заемане на академична длъжност доцент по специалност 4.1 физически науки/квантова информатика/ обявен в ДВ бр.102 от 12.12.2014 г. с единствен кандидат Петър Александров Иванов,
РЕЦЕНЗИЯ
 До Секцията по Обща микробиология към Институт по микробиология Стефан Ангелов при Българската Академия на Науките Р Е Ц Е Н З И Я на дисертационен труд Ко-агрегация между щамове Bacillus subtilis и Escherichia
До Секцията по Обща микробиология към Институт по микробиология Стефан Ангелов при Българската Академия на Науките Р Е Ц Е Н З И Я на дисертационен труд Ко-агрегация между щамове Bacillus subtilis и Escherichia
Microsoft Word - Ucheben plan_HimiaiFizika_bachelor.doc
 С О Ф И Й С К И У Н И В Е Р С И Т Е Т СВ. К Л И М Е Н Т О Х Р И Д С К И УЧЕБЕН ПЛАН Утвърждавам, Професионално направление: ПЕДАГОГИКА НА ОБУЧЕНИЕТО ПО (подпис) Специалност: ХИМИЯ И ФИЗИКА Образователно-
С О Ф И Й С К И У Н И В Е Р С И Т Е Т СВ. К Л И М Е Н Т О Х Р И Д С К И УЧЕБЕН ПЛАН Утвърждавам, Професионално направление: ПЕДАГОГИКА НА ОБУЧЕНИЕТО ПО (подпис) Специалност: ХИМИЯ И ФИЗИКА Образователно-
The Cell
 Клетка 1.Клетката основна структурна и функционална единица на живия организъм 2.Прокариотни и еукариотни клетки 3.Клетъчна организация: външна морфология на клетката големина, форма и цвят на клетките
Клетка 1.Клетката основна структурна и функционална единица на живия организъм 2.Прокариотни и еукариотни клетки 3.Клетъчна организация: външна морфология на клетката големина, форма и цвят на клетките
РЕЦЕНЗИЯ
 1 РЕЦЕНЗИЯ от проф. дхн ТЕМЕНУЖКА НЕЙЧЕВА КОНСТАНТИНОВА, ХТМУ по конкурс за заемане на академичната длъжност доцент, научна специалност 5.10 Химични технологии (Технология на финия органичен и биохимичен
1 РЕЦЕНЗИЯ от проф. дхн ТЕМЕНУЖКА НЕЙЧЕВА КОНСТАНТИНОВА, ХТМУ по конкурс за заемане на академичната длъжност доцент, научна специалност 5.10 Химични технологии (Технология на финия органичен и биохимичен
16. НЯКОИ НЕРАВНОВЕСНИ И НЕЛИНЕЙНИ ЯВЛЕНИЯ В КРИСТАЛИТЕ ТОПЛОПРОВОДНОСТ, ЕЛЕКТРОПРОВОДИМОСТ, ЕЛЕКТРОСТРИКЦИЯ. ТЕРМОЕЛЕКТРИЧНИ ЕФЕКТИ 1. Нелинейни или
 16. НЯКОИ НЕРАВНОВЕСНИ И НЕЛИНЕЙНИ ЯВЛЕНИЯ В КРИСТАЛИТЕ ТОПЛОПРОВОДНОСТ, ЕЛЕКТРОПРОВОДИМОСТ, ЕЛЕКТРОСТРИКЦИЯ. ТЕРМОЕЛЕКТРИЧНИ ЕФЕКТИ 1. Нелинейни или квадратични ефекти 1.1. Електрострикция При голяма
16. НЯКОИ НЕРАВНОВЕСНИ И НЕЛИНЕЙНИ ЯВЛЕНИЯ В КРИСТАЛИТЕ ТОПЛОПРОВОДНОСТ, ЕЛЕКТРОПРОВОДИМОСТ, ЕЛЕКТРОСТРИКЦИЯ. ТЕРМОЕЛЕКТРИЧНИ ЕФЕКТИ 1. Нелинейни или квадратични ефекти 1.1. Електрострикция При голяма
ИЗСЛЕДВАНЕ НА КИНЕТИКАТА НА ОСАПУНВАНЕ НА ЕТИЛАЦЕТАТ Цел: Да се изследва кинетиката на осапунване на етилацетат с натриева основа. Теоретична част: Ре
 ИЗСЛЕДВАНЕ НА КИНЕТИКАТА НА ОСАПУНВАНЕ НА ЕТИЛАЦЕТАТ Цел: Да се изследва кинетиката на осапунване на етилацетат с натриева основа. Теоретична част: Реакцията на осапунване на етилацетат с натриева основа
ИЗСЛЕДВАНЕ НА КИНЕТИКАТА НА ОСАПУНВАНЕ НА ЕТИЛАЦЕТАТ Цел: Да се изследва кинетиката на осапунване на етилацетат с натриева основа. Теоретична част: Реакцията на осапунване на етилацетат с натриева основа
Рецензия във връзка с конкурс за заемане на академичната длъжност професор в област на висше образование 4. Природни науки, математика и информатика,
 Рецензия във връзка с конкурс за заемане на академичната длъжност професор в област на висше образование 4. Природни науки, математика и информатика, професионално направление 4.2. Химически науки (Теоретична
Рецензия във връзка с конкурс за заемане на академичната длъжност професор в област на висше образование 4. Природни науки, математика и информатика, професионално направление 4.2. Химически науки (Теоретична
