МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА РЕГИОНАЛНO УПРАВЛЕНИЕ НА ОБРАЗОВАНИЕТО СОФИЯ-ГРАД София 1303, ул. Антим I, 17, тел.: , факс: , e-m
|
|
|
- Vangelia Tscharyiski
- преди 5 години
- Прегледи:
Препис
1 МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА РЕГИОНАЛНO УПРАВЛЕНИЕ НА ОБРАЗОВАНИЕТО СОФИЯ-ГРАД София 1303, ул. Антим I, 17, тел.: , факс: , Подборен кръг за XХ -то Национално състезание по химия и опазване на околната среда г. Част I 1. Коя от следните частици НЕ може да участва в образуването на донорно-акцепторна връзка? H H А) H C H Б) H N В) - Г) H + H H 2. За коя от посочените двойки частици е вярно, че имат завършен външен електронен слой с осем електрона? А) Hˉ и He Б) Ca и K + В) Аl 3+ и В 3+ Г) Clˉ и Ca Кой от газовете може да се получи и събере по дадената схема? А) NO 2 от твърд Cu(NO 3) 2 Б) NH 3 от твърд NH 4Cl В) O 2 от твърд KClO 3 Г) CO 2 от твърд CaCO 3 4. Газообразно вещество X с маса 32,4 g при 0 0 С и налягане Ра заема обем 8,96 dm 3. Коя от формулите съответства на Х? А) Kr Б) HBr В) Cl 2 Г) O 3 5. При взаимодействие на диалуминиев триоксид с концентриран разтвор на натриева основа, продуктите са: А) Na 3[Al() 6] и Н 2 Б) Na 3[Al() 6] В) NaAlO 2 и Н 2 Г) NaAlO 2 6. От коя група всички означени веществата реагират с вода? А) MgO, SiO 2, H 2CO 3 В) Na 2O, Cl 2, CaH 2 Б) Al 2O 3, SO 2, HNO 3 Г) CuSO 4, CO 2, HCI 7. При кое от означените взаимодействия водородът се проявява и като окислител, и като редуктор? А) H 2 + CuO t В) NaH + Cl 2 Б) CaH 2 + HCl Г) CH 4 + H 2O p,t 8. Водородът, необходим за производството на амоняк се получава от природен газ по реакцията: CH 4(г) + H 2O (г) CO (г) + 3 H 2(г) 207 kj. Кое от посочените условия води до получаването на по-голямо количество водород? А) понижаване на температурата и понижаване на налягането Б) понижаване на температурата и повишаване на налягането В) повишаване на температурата и понижаване на налягането Г) повишаване на температурата и повишаване на налягането 9. Взаимодействието между CH 3 и CH 3CO е: А) хидролиза Б) дехидратация В) неутрализация Г) естерификация 1
2 10. Топлинният ефект на коя от означeните с термохимични уравнения реакции е топлина на изгаряне: А) S (тв) + O 2(г) SO 2(г) + Q Б) C (диамант) + O 2(г) CO 2 (г) + Q В) 2 H 2(г) + О 2(г) 2 H 2O (г) + Q Г) 4 P (червен) + 5 О 2(г) 2 P 2O 5 (тв)+ Q бутин може да се различи от 2-бутин по взаимодействито с: А) разтвор на бром в CCl 4 Б) KMnO 4 в сярнокисела среда В) натрий в течен амоняк Г) вода 12. Взаимодействието между веществата А и В в газова фаза 2А + В А 2В + Q преминава през етапите: (1) А + В АВ + Q 1 (бавен) (2) АВ + А А 2В - Q 2 (бърз) Кинетичното уравнение на реакцята е: А) v = k.c 2 (A).c(B) Б) v = k.c(a).c(b) В) v = k.c(a 2B) Г) v = k.c(ab).c(a) 13. Молната концентрация на разтвор, получен при смесването на 400 ml 6M HCl и 200 cm 3 2M HCl e: А) 8 mol/l Б) 4,7 mol/l В) 4,4 mol/l Г) 4 mol/l 14. Кое е веществото Х, ако е известно, че 1 mol от него взаимодейства с 2 mol натриева основа и обезцветява бромна вода? А) салицилова киселина Б) млечна киселина В) фенол Г) глюкоза 15. В четири епруветки има разтвори на етанол, ацетон, глицерол, глюкоза. С кой от изброените реактиви ще разпознаете еднозначно глюкозата? А) разтвор на KMnO 4 в сярнокисела среда Б) I 2 и Na, при нагряване В) прясно утаен Cu() 2 при стайна температура Г) прясно утаен Cu() 2 при нагряване 16. За демонстрация г-жа Петрова трябвало да получи водород. Използвала цинк на гранули и разредена сярна киселина. Скоростта на реакцията Zn + H 2 SO 4 А) добави още от сярната киселина Б) добави вода В) понижи температурата Г) използва цинк на прах ZnSO 4 + H 2 ще се увеличи, ако се: 17. В кой от редовете всички вещества са подредени по засилване на киселинните им свойства: А) CH 3 < C 6H 5 < H 2O < CH 3CO< C 6H 5CO Б) CH 3 < H 2O < C 6H 5 < CH 3CO < ClCO В) HCO > CH 3CO > H 2CO 3 > H 2O > C 2H 5 Г) H 2CO 3 > HCO > CH 3CO > C 6H 5 > C 2H С разтвор на KMnO 4 НЕ реагира: А) етанол Б) толуен В) акрилова киселина Г) стеаринова киселина 2
3 19. Кое от означените взаимодействия е НЕВЪЗМОЖНО? А) C 17H 33CO + Na Б) CH 3COCH 3 + Cu() 2 t В) CH 3COCH 3 + HCN Г) CH 3CHO + [Ag(NH 3) 2] t 20. Посочете вярното твърдение: Амилопектинът: А) се разтваря добре в гореща вода. Б) има разклонена макромолекула. В) не се хидролизира на степени. Г) е линеен полимер, изграден от -глюкозни остатъци. 21. За съединението Х се знае, че: реагира с Na и K; не се окислява и не реагира с основи; при взаимодействие с оцетна киселина образува продукт със състав CH 3COOC 4H 9. Кое е химичното съединение Х? А) CH 3CH()CH 3 Б) (CH 3) 3C В) CH 3 Г) CH 3CO 22. Веществото Y взаимодейства с прясно утаен меден дихидроксид при нагряване и се +H 2 O, p, t О 2, 300, Cu получава по схемата: C 3H 7Cl X Y. Коя е структурната формула на веществото Y? A) CH 3COCH 3 Б) CH 3CH()CH 3 В) CH 3 Г) CH 3CHO 23. Кои са продуктите при алкална хидролиза на фенилетаноат? А) СН 3СH 2ONa и C 6H 5CO Б) СН 3СH 2ОH и C 6H 5COONa В) СН 3COONa и C 6H 5 Г) СН 3COOН и C 6H 5ОNa 24. Кое от следните вещества може да участва както в процес на поликондензация, така и в процес на полимеризация? А) HOСН 2 СН 2OН Б) СН 2=СН СН=СН 2 В) HСНO Г) HOOС(CН 2) 4СO 25. Оптична изомерия проявява съединението: А) 2-аминоетанова киселина Б) 3-аминопропанова киселина В) 3-бромо-2-бутанон Г) 2-метил-2-хлоропропанал 3
4 МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА РЕГИОНАЛНO УПРАВЛЕНИЕ НА ОБРАЗОВАНИЕТО СОФИЯ-ГРАД София 1303, ул. Антим I, 17, тел.: , факс: , Подборен кръг за XХ -то Национално състезание по химия и опазване на околната среда г. Част II Задача 26 7 точки Простото вещество А е електро- и топлопроводимо. При взаимодействие на А със солна киселина в присъствие на водороден пероксид се получава сол Б. При прибавяне на калиева основа към воден разтвор на Б се образува светлосиня утайка В, частично разтворима в излишък на утаителя. Утайката В се разтваря в амонячна вода - получава се мастиленосин разтвор - Г. А) Кои са веществата А, Б, В и Г? Запишете формулите им! А... В... Б... Г... Б) Означете с уравнения получаването на солта Б и взаимодействието й с разтвор на калиева основа. Определете вида на процесите и ги изразете по подходящ начин. В) Обяснете чрез уравнение защо утайката В се разтваря в амоняк? Г) Какви продукти се получават при електролиза във воден разтвор на В? Запишете само продуктите БЕЗ да изразявате процесите с уравнения! Продукти на анода:... Продукти на катода:... 4
5 Задача 27 7 точки На фигурата е представена графично разтворимостта на някои твърди вещества като функция от температурата. За лабораторна работа са необходими разтвори на оловен динитрат и на амониев хлорид. А) Определете разтворимостта тези соли в 100 g вода при 50 о С и при 90 о С. Соли Разтворимост в 100 g вода при Pb(NO 3) 2 NH 4Cl 50 С 80 С Б) Kакъв е топлинният ефект на процеса разтваряне на Pb(NO 3) 2?... Обосновете отговора си! Фиг 1. Разтворимост на някои твърди вещества в 100 g вода при различни температури В) Изчислете масовата част на Pb(NO 3) 2 в наситения при 50 о С разтвор. Г) Какъв характер има водният разтвор на NH 4Cl? Изразете процеса със съкратено йонно уравнение! 5
6 Задача 28 8 точки Един от етапите при производството на сярна киселина е окислението на серен диоксид до серен триоксид. При определена температура в затворен съд се установява равновесие при следните молни концентрации: c(so2) = 0,8 mol/l, c(o2) = 0,6 mol/l, c(so3) = 1,2 mol/l. А) Изразете процеса с уравнение и запишете израза за равновесната константа Kc. Б) Изчислете стойността на равновесната константа Kc и началните концентрации на серния диоксид и на кислорода. В) Изчислете топлинния ефект на реакцията, ако знаете, че топлините на образуване на двата оксида са Q o (SO2) = 297 kj/mol, Q o (SO3) = 443 kj/mol. Г) Как ще се промени равновесната концентрация на кислорода, ако: се понижи налягането; се понижи температурата? Обосновете кратко отговорите си! Понижаване на налягането Понижение на температурата Д) Запишете израза за кинетичното уравнение на правата реакция и определете нейния порядък. Приемете, че реакцията протича по даденото уравнение. 6
7 Задача 29 8 точки При алкална хидролиза на триглицерида Y се получават веществото А и солта Б. Триглицеридът Y се получава от Х чрез реакция на хидрогениране. А) Запишете формулите на триглицеридите X и Y, ако е известно, че: - относителната молекулна маса на Х е с 4 по-малка от тази на Y; - при киселинна хидролиза на X се получават веществото А и смес от киселините В и Г в съотношение 2 : 1; - Двете киселини са с по 18 C-атома; киселината В обезцветява разтвор на бром в CCl4, а Г не реагира с разтвор на КМnО4. X Y Б) Означете с уравнения алкалната хидролиза Y (с разтвор на K) и получаването му от Х. В) Кое е веществото А? Опишете качествена реакция за доказването му. Г) Какви промени ще се наблюдават, ако към разтвор на солта Б се добави разтвор на MgCl2. Обосновете отговора си с подходящо уравнение. Д) Колко грама 2%-ен разтвор на бром в CCl4 са необходими за пълното взаимодействие с 0,02 mol от X? 7
8 Задача 30 9 точки Парацетамолът е широко употребявано лекарство от групата на нестероидните противовъзпалителни средства. Изходно вещество за получаването му е 4-аминофенол. А) Какво е отнасянето на 4-аминофенол към натриева основа, концентрирана солна киселина и бромна вода? Означете с уравнения и обяснете възможните взаимодействия. Б) Парацетамолът се получава при нагряване на 4-аминофенол с оцетен анхидрид в съотношение 1 : 1. Напишете уравнението на получаването му, ако е известно, че парацетамолът дава виолетово оцветяване с воден разтвор на FeCl3. В) При взаимодействието на 4-аминофенола с оцетен анхидрид в съотношение 1 : 2 при кипене се получава друг продукт. Напишете уравнението. Г) Оцетният анхидрид може да се получи от природен газ по схемата: А 2000 Б + H 2O, Hg 2+ (H 2 SO 4 ) В Г P 2O 5, t оцетен анхидрид Кои са веществата А, Б, В и Г? Запишете формулите им. А... В... Б... Г... 8
9 МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА РЕГИОНАЛНO УПРАВЛЕНИЕ НА ОБРАЗОВАНИЕТО СОФИЯ-ГРАД София 1303, ул. Антим I, 17, тел.: , факс: , ПРИМЕРНИ РЕШЕНИЯ Подборен кръг за XХ -то Национално състезание по химия и опазване на околната среда 2019 г. Част I Тест 25 зад. х = 25 т. Зад. Отговори Зад. Отговори Зад. Отговори 1 A Б В Г 11 A Б В Г 21 A Б В Г 2 A Б В Г 12 A Б В Г 22 A Б В Г 3 A Б В Г 13 A Б В Г 23 A Б В Г 4 A Б В Г 14 A Б В Г 24 A Б В Г 5 A Б В Г 15 A Б В Г 25 A Б В Г 6 A Б В Г 16 A Б В Г 7 A Б В Г 17 A Б В Г 8 A Б В Г 18 A Б В Г 9 A Б В Г 19 A Б В Г 10 A Б В Г 20 A Б В Г 9
10 Част II Задача 26 7 точки А) А - Cu Б CuCl 2 В Cu() 2 Г [CuNH 3) 2]() 2 4 х 0,25 т. = 1,0 т. Б) Cu + H 2O HCl CuCl H 2O с електронен баланс = 2 т. CuCl К Cu() КCl Пълно йонно уравнение Съкратено йонно ураевнение 1,0 т. В) Cu() NH 3 [Cu(NH 3) 2]() 2 Г) Катод Cu Aнод Cl 2 2 х = Задача 27 7 точки А) Соли Разтворимост в 100 g вода при 50 С 80 С Pb(NO 3) NH 4Cl Б) Ендотермичен. С увеличаване на температурата (съгласно принципа на Льо Шателие- Браун) протича ендотермичната реакция. С увеличаване на температурата разтворимостта на Pb(NO 3) 2 расте. В) w(pb(no 3 ) 2 ) = m(pb(no 3) 2 ) m Г) За съкратеното йонно уравнение c(h + ) > c ( - ), киселинен, рн < 7 = 4 х = 2,0 т. 80 = 0,4444 или 44,44 % 1,5 т Задача 28 8 точки А) 2 SO 2 + O 2 2 SO 3 c 2 (SO 3 ) K c = c(o 2 ). c 2 (SO 2 ) Б) 1,2 2 K c = 0,8 2. 0,6 = 3,75 c 0(SO 2) = c реаг.(so 2) + c(so 2) = 1, = 2 mol c 0(O 2) = c реаг.(o 2) + c(o 2) = 0,6 + 0,6 = 1,2 mol В) Q = 2Q o (SO 3) - 2 Q o (SO 2) = 2(Q o (SO 3) - Q o (SO 2)) = 2 ( ) = 292 kj Q o (O 2) = 0 kj/mol Г) Намаляване на налягането протича обратната реакция, c(o 2) нараства (с обяснение) Понижение на температурата протича правата реакция, c(o 2) намалява (с обяснение) v = kc 2 (SO 2).c(O 2). Общият порядък на реакцията - трети. 0,75 т. 0,75 т. 1,5 т. 1,5 т. 0,75 т. 0,25 т. 10
11 Задача 29 А) 8 точки H 33 H 33 2 х = 2 т. CH H 33 CH CH Б) CH X 2 CH или 2 H 33 CH Y 2 CH + 3 K t o CH + 3 C 17 COOK 2 x = 2т. В) Г) Д) H 33 CH H Ni, p, t H 2 o CH А C 3H 5() 3, глицерол Взаимодействие с Cu() 2 - тъмносиньо оцветяване Б C 17COOК, калиев стеарат 2 C 17COO - +2 К + + Mg Cl - (C 17COO) 2Mg +2 К Cl - Получава се утайка (сапунът се пресича) n(x) : n(br 2) = 1 : 2 n(br 2) = 2 n(x) = 2x0,02 = 0,04 mol m = m(br 2) w(br 2 ) = n(br 2). M(Br 2 ) = 0, = 320 g w(br 2 ) 0,02 Задача 30 A) 9 точки ONa 3 х = 3 т. + Na + H 2 O + HCl + 2 Br 2 Б) + (CH 3 CO) 2 O + - NH 3 Cl Br HBr Br 2 т. t o + CH 3 CO В) + 2 (CH 3 CO) 2 O NHCOCH 3 OOCCH CH 3 CO 2 т. NHCOCH 3 Г) А CH 4 В CH 3CHO 4 х 0,5т. = 2 т. Б HC CH Г CH 3CO 11
ХИМИЯ
 ХИМИЯ (2009) Националност Име Презиме Фамилия (Моля, напишете с печатни букви тритете си имена, като подчертаете фамилното си име) Оценки І Напишете номера на правилния отговор в съответната клетка за
ХИМИЯ (2009) Националност Име Презиме Фамилия (Моля, напишете с печатни букви тритете си имена, като подчертаете фамилното си име) Оценки І Напишете номера на правилния отговор в съответната клетка за
Изпитни въпроси и задачи
 Въпроси ВАРИАНТ II ТЕСТ 1 Коя от посочените електронни формули е вярна? а) 1s 2 2s 2 2p 5 3s 2 ; в) 1s 2 2s 2 2p 6 3s 2 ; д) 1s 2 1p 2 2p 6 3s 2 б) 1s 2 2s 2 2p 3 3s 1 ; г) 1s 2 2s 2 2p 5 2d 2 ; 2 В молекулата
Въпроси ВАРИАНТ II ТЕСТ 1 Коя от посочените електронни формули е вярна? а) 1s 2 2s 2 2p 5 3s 2 ; в) 1s 2 2s 2 2p 6 3s 2 ; д) 1s 2 1p 2 2p 6 3s 2 б) 1s 2 2s 2 2p 3 3s 1 ; г) 1s 2 2s 2 2p 5 2d 2 ; 2 В молекулата
химия Използвайте следните стойности : ("L" означава литри) Универсална газова константа: R = 8, Ра.L1(к.mоl) = 8,31 J/(к.mоl) = 0,082 аtm.l1(к.
 химия Използвайте следните стойности : ("L" означава литри) Универсална газова константа: R = 8,31.103 Ра.L1(к.mоl) = 8,31 J/(к.mоl) = 0,082 аtm.l1(к.mоl) Число на Авогадро: N A = 6,0.1023 mol Стандартни
химия Използвайте следните стойности : ("L" означава литри) Универсална газова константа: R = 8,31.103 Ра.L1(к.mоl) = 8,31 J/(к.mоl) = 0,082 аtm.l1(к.mоl) Число на Авогадро: N A = 6,0.1023 mol Стандартни
ПРИМЕРЕН ТЕСТ (компонент 1) 1 Коя от следните електронни формули е вярна? а) 1s 2 2s 2 2p 5 3s 2 ; б) 1s 2 2s 2 2p 3 3s 1 ; в) 1s 2 2s 2 2p 6 3s 2 ; г
 ПРИМЕРЕН ТЕСТ (компонент 1) 1 Коя от следните електронни формули е вярна? а) 1s 2 2s 2 2p 5 3s 2 ; б) 1s 2 2s 2 2p 3 3s 1 ; в) 1s 2 2s 2 2p 6 3s 2 ; г) 1s 2 2s 2 2p 5 2d 2 ; д) 1s 2 1p 2 2p 6 3s 2 2 В
ПРИМЕРЕН ТЕСТ (компонент 1) 1 Коя от следните електронни формули е вярна? а) 1s 2 2s 2 2p 5 3s 2 ; б) 1s 2 2s 2 2p 3 3s 1 ; в) 1s 2 2s 2 2p 6 3s 2 ; г) 1s 2 2s 2 2p 5 2d 2 ; д) 1s 2 1p 2 2p 6 3s 2 2 В
КСК'14
 Въпроси ХИМИЯ I (26 април 2015 год.) ТЕСТ 1 Коя от следните електронни формули е правилно записана за атом на химичен елемент? а) 1s 2 2s 2 2p 3 3s 2 ; в) 1s 2 1p 6 2s 3 2p 6 ; д) 1s 2 2s 2 2p 6 3s 2 3p
Въпроси ХИМИЯ I (26 април 2015 год.) ТЕСТ 1 Коя от следните електронни формули е правилно записана за атом на химичен елемент? а) 1s 2 2s 2 2p 3 3s 2 ; в) 1s 2 1p 6 2s 3 2p 6 ; д) 1s 2 2s 2 2p 6 3s 2 3p
КСК'17
 енергия Въпроси ТЕСТ ХИМИЯ II (15.06.2019) 1 Коя комбинация от квантови числа е възможна? а) n = 4, l = 4, m = -3 б) n = 4, l = 1, m = 2 в) n = 3, l = -2, m = 2 г) n = 2, l = 1, m = -1 д) n = 1, l = 2,
енергия Въпроси ТЕСТ ХИМИЯ II (15.06.2019) 1 Коя комбинация от квантови числа е възможна? а) n = 4, l = 4, m = -3 б) n = 4, l = 1, m = 2 в) n = 3, l = -2, m = 2 г) n = 2, l = 1, m = -1 д) n = 1, l = 2,
КСК'14
 УКАЗАНИЯ За проверка и оценка на кандидат-студентските работи по Химия - предварителен изпит - 6.4.15 г. за учебната 15/16 г. - ОБЩИ ПОЛОЖЕНИЯ9 Задачите са от материала по обща, неорганична и органична
УКАЗАНИЯ За проверка и оценка на кандидат-студентските работи по Химия - предварителен изпит - 6.4.15 г. за учебната 15/16 г. - ОБЩИ ПОЛОЖЕНИЯ9 Задачите са от материала по обща, неорганична и органична
9 клас
 H X C H Fe Si C МОН, LI НАЦИОНАЛНА ОЛИМПИАДА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА Областен кръг, 10 февруари 019 г. Учебно съдържание X - XII клас Примерни решения и оценка на задачите Важно за проверителите!
H X C H Fe Si C МОН, LI НАЦИОНАЛНА ОЛИМПИАДА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА Областен кръг, 10 февруари 019 г. Учебно съдържание X - XII клас Примерни решения и оценка на задачите Важно за проверителите!
Изпитни въпроси и задачи
 УКЗНИЯ За проверка и оценка на кандидат-студентските работи по Химия II - 13.6.15 г. за учебната 15/16 г. I. ОБЩИ ПОЛОЖЕНИЯ: Задачите са от материала по обща, неорганична и органична химия според учебниците
УКЗНИЯ За проверка и оценка на кандидат-студентските работи по Химия II - 13.6.15 г. за учебната 15/16 г. I. ОБЩИ ПОЛОЖЕНИЯ: Задачите са от материала по обща, неорганична и органична химия според учебниците
Въпроси ТЕСТ ХИМИЯ I ( г.) 1 Коя от електронните формули на атом в основно състояние НЕ е вярна? а) 1s 2 2s 2 2p 4 б) 1s 2 2s 2 2p 6 3s 1 в)
 Въпроси ТЕСТ ХИМИЯ I (21.04.2019 г.) 1 Коя от електронните формули на атом в основно състояние НЕ е вярна? а) 1s 2 2s 2 2p 4 б) 1s 2 2s 2 2p 6 3s 1 в) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 2 г) 1s 2 2s 2 2p 6 3s
Въпроси ТЕСТ ХИМИЯ I (21.04.2019 г.) 1 Коя от електронните формули на атом в основно състояние НЕ е вярна? а) 1s 2 2s 2 2p 4 б) 1s 2 2s 2 2p 6 3s 1 в) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 2 г) 1s 2 2s 2 2p 6 3s
М И Н И С Т Е Р С Т В О Н А О Б Р А З О В А Н И Е Т О И Н А У К А Т А ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 28 май 2009 г. Ва
 М И Н И С Т Е Р С Т В О Н А О Б Р А З О В А Н И Е Т О И Н А У К А Т А ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 28 май 2009 г. Вариант 2 УВАЖАЕМИ ЗРЕЛОСТНИЦИ, Пред Вас е тестът за
М И Н И С Т Е Р С Т В О Н А О Б Р А З О В А Н И Е Т О И Н А У К А Т А ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 28 май 2009 г. Вариант 2 УВАЖАЕМИ ЗРЕЛОСТНИЦИ, Пред Вас е тестът за
МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 30 май 2019 г. Вариант 1 МОДУЛ 1 Време за работ
 МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 30 май 2019 г. Вариант 1 МОДУЛ 1 Време за работа 90 минути Отговорите на задачите от 1. до 35. вкл.
МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО И НАУКАТА ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 30 май 2019 г. Вариант 1 МОДУЛ 1 Време за работа 90 минути Отговорите на задачите от 1. до 35. вкл.
МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО, МЛАДЕЖТА И НАУКАТА ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 23 май 2011 г. Вариант 2 УВАЖАЕМИ ЗРЕ
 МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО, МЛАДЕЖТА И НАУКАТА ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 23 май 2011 г. Вариант 2 УВАЖАЕМИ ЗРЕЛОСТНИЦИ, Тестът съдържа 50 задачи по химия и опазване
МИНИСТЕРСТВО НА ОБРАЗОВАНИЕТО, МЛАДЕЖТА И НАУКАТА ДЪРЖАВЕН ЗРЕЛОСТЕН ИЗПИТ ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА 23 май 2011 г. Вариант 2 УВАЖАЕМИ ЗРЕЛОСТНИЦИ, Тестът съдържа 50 задачи по химия и опазване
ИЗСЛЕДВАНЕ НА КИНЕТИКАТА НА ОСАПУНВАНЕ НА ЕТИЛАЦЕТАТ Цел: Да се изследва кинетиката на осапунване на етилацетат с натриева основа. Теоретична част: Ре
 ИЗСЛЕДВАНЕ НА КИНЕТИКАТА НА ОСАПУНВАНЕ НА ЕТИЛАЦЕТАТ Цел: Да се изследва кинетиката на осапунване на етилацетат с натриева основа. Теоретична част: Реакцията на осапунване на етилацетат с натриева основа
ИЗСЛЕДВАНЕ НА КИНЕТИКАТА НА ОСАПУНВАНЕ НА ЕТИЛАЦЕТАТ Цел: Да се изследва кинетиката на осапунване на етилацетат с натриева основа. Теоретична част: Реакцията на осапунване на етилацетат с натриева основа
Microsoft Word - Vas_25a.doc
 126 АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА 25. АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА Полярната група на АПАВ, която чрез дисоциирането си придава водоразтворимост на цялата молекула, може да бъде COONa, OSO3Na
126 АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА 25. АНИОННИ ПОВЪРХНОСТНОАКТИВНИ ВЕЩЕСТВА Полярната група на АПАВ, която чрез дисоциирането си придава водоразтворимост на цялата молекула, може да бъде COONa, OSO3Na
ОПРЕДЕЛЯНЕ НА РАВНОВЕСНА КОНСТАНТА НА ХОМОГЕННА РЕАКЦИЯ В РАЗТВОР Състоянието на системата от реагиращи вещества, при което скоростите на правата и об
 ОПРЕДЕЛЯНЕ НА РАВНОВЕСНА КОНСТАНТА НА ХОМОГЕННА РЕАКЦИЯ В РАЗТВОР Състоянието на системата от реагиращи вещества, при което скоростите на правата и обратната реакция са равни, а съставът на системата не
ОПРЕДЕЛЯНЕ НА РАВНОВЕСНА КОНСТАНТА НА ХОМОГЕННА РЕАКЦИЯ В РАЗТВОР Състоянието на системата от реагиращи вещества, при което скоростите на правата и обратната реакция са равни, а съставът на системата не
УКАЗАНИЯ ЗА ПРОВЕРКА И ОЦЕНКА НА ПИСМЕНИТЕ КАНДИДАТ-СТУДЕНТСКИ РАБОТИ ПО ХИМИЯ ЗА УЧЕБНАТА 2014/2015 г В МУ-ПЛЕВЕН I. ОБЩИ ПОЛОЖЕНИЯ. Преглеждането и
 УКАЗАНИЯ ЗА ПРОВЕРКА И ОЦЕНКА НА ПИСМЕНИТЕ КАНДИДАТ-СТУДЕНТСКИ РАБОТИ ПО ХИМИЯ ЗА УЧЕБНАТА 2014/2015 г В МУ-ПЛЕВЕН I. ОБЩИ ПОЛОЖЕНИЯ. Преглеждането и оценяването на писмените работи се извършват в съответствие
УКАЗАНИЯ ЗА ПРОВЕРКА И ОЦЕНКА НА ПИСМЕНИТЕ КАНДИДАТ-СТУДЕНТСКИ РАБОТИ ПО ХИМИЯ ЗА УЧЕБНАТА 2014/2015 г В МУ-ПЛЕВЕН I. ОБЩИ ПОЛОЖЕНИЯ. Преглеждането и оценяването на писмените работи се извършват в съответствие
КАНДИДАТСТУДЕНТСКИ ИЗПИТ по Химия за специалностите "Медицина", "Дентална медицина" и "Фармация" г. Неорганична химия 1. Главното квантово
 КАНДИДАТСТУДЕНТСКИ ИЗПИТ по Химия за специалностите "Медицина", "Дентална медицина" и "Фармация" 08.07.2019 г. Неорганична химия 1. Главното квантово число n определя: a. енергията на електрона и размерите
КАНДИДАТСТУДЕНТСКИ ИЗПИТ по Химия за специалностите "Медицина", "Дентална медицина" и "Фармация" 08.07.2019 г. Неорганична химия 1. Главното квантово число n определя: a. енергията на електрона и размерите
... (Училище) УТВЪРДИЛ Директор:... (Име, фамилия, подпис) ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 9.
 ... (Училище) УТВЪРДИЛ Директор:... (Име, фамилия, подпис) ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 9. клас Брой учебни часове (по учебен план): 54. За нови
... (Училище) УТВЪРДИЛ Директор:... (Име, фамилия, подпис) ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 9. клас Брой учебни часове (по учебен план): 54. За нови
II
 УТВЪРДИЛ: Директор:... (Име, фамилия, подпис) ПРИМЕРНО ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 10. клас Брой учебни часове (по учебен план): 72. Брой часове
УТВЪРДИЛ: Директор:... (Име, фамилия, подпис) ПРИМЕРНО ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 10. клас Брой учебни часове (по учебен план): 72. Брой часове
УЧЕБНА ПРОГРАМА ПО ФИЗИКА И АСТРОНОМИЯ 11 КЛАС ЗИП
 УЧЕБНА ПРОГРАМА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА ЗА VII КЛАС (ОБЩООБРАЗОВАТЕЛНА ПОДГОТОВКА) Приложение 29 към т. 29 КРАТКО ПРЕДСТАВЯНЕ НА УЧЕБНАТА ПРОГРАМА Учебната програма по химия и опазване на
УЧЕБНА ПРОГРАМА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА ЗА VII КЛАС (ОБЩООБРАЗОВАТЕЛНА ПОДГОТОВКА) Приложение 29 към т. 29 КРАТКО ПРЕДСТАВЯНЕ НА УЧЕБНАТА ПРОГРАМА Учебната програма по химия и опазване на
ПРОГРАМА за кандидат-студентския изпит по Химия за специалността Медицина Университет Проф. д-р А. Златаров -бургас 1. Строеж на атома. 2. Периодичен
 ПРОГРАМА за кандидат-студентския изпит по Химия за специалността Медицина Университет Проф. д-р А. Златаров -бургас 1. Строеж на атома. 2. Периодичен закон и периодична система на химичните елементи. 3.
ПРОГРАМА за кандидат-студентския изпит по Химия за специалността Медицина Университет Проф. д-р А. Златаров -бургас 1. Строеж на атома. 2. Периодичен закон и периодична система на химичните елементи. 3.
TEMA 3 Химична връзка Част 1.1. Химична връзка исторически аспекти на теорията Какво трябва да знам? определение за химична връзка; класическите предс
 TEMA 3 Химична връзка Част 1.1. Химична връзка исторически аспекти на теорията определение за химична връзка; класическите представи на Люис и Косел за причината за образуване на химична връзка Част 1.2.Ковалентна
TEMA 3 Химична връзка Част 1.1. Химична връзка исторически аспекти на теорията определение за химична връзка; класическите представи на Люис и Косел за причината за образуване на химична връзка Част 1.2.Ковалентна
МОМН, 45-та НАЦИОНАЛНА ОЛИМПИАДА
 H X C H Fe Si C МОН, LI НАЦИОНАЛНА ОЛИМПИАДА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА Областен кръг, 10 февруари 2019 г. Учебно съдържание VIII клас Уважаеми ученици, предстои Ви да решите тест от две части.
H X C H Fe Si C МОН, LI НАЦИОНАЛНА ОЛИМПИАДА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА Областен кръг, 10 февруари 2019 г. Учебно съдържание VIII клас Уважаеми ученици, предстои Ви да решите тест от две части.
СЪДЪРЖАНИЕ НАЧАЛЕН ПРЕГОВОР Метали, неметали и техните съединения...7 Екологични проблеми...8 Величини и зависимости...9 Въглерод. Въглеводороди...10
 СЪДЪРЖАНИЕ НАЧАЛЕН ПРЕГОВОР Метали, неметали и техните съединения...7 Екологични проблеми...8 Величини и зависимости...9 Въглерод. Въглеводороди...10 Производни на въглеводородите... 11 Входно равнище
СЪДЪРЖАНИЕ НАЧАЛЕН ПРЕГОВОР Метали, неметали и техните съединения...7 Екологични проблеми...8 Величини и зависимости...9 Въглерод. Въглеводороди...10 Производни на въглеводородите... 11 Входно равнище
Microsoft Word - UP_HIM_PP_11 kl_M1
 Приложение 113 към т. 113 УЧЕБНА ПРОГРАМА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА (ПРОФИЛИРАНА ПОДГОТОВКА) МОДУЛ 1. ТЕОРЕТИЧНИ ОСНОВИ НА ХИМИЯТА КРАТКО ПРЕДСТАВЯНЕ НА УЧЕБНАТА ПРОГРАМА Модулът Теоретични
Приложение 113 към т. 113 УЧЕБНА ПРОГРАМА ПО ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА (ПРОФИЛИРАНА ПОДГОТОВКА) МОДУЛ 1. ТЕОРЕТИЧНИ ОСНОВИ НА ХИМИЯТА КРАТКО ПРЕДСТАВЯНЕ НА УЧЕБНАТА ПРОГРАМА Модулът Теоретични
Училище:, град/село... Утвърдил директор:.. (име, фамилия, подпис) ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната сре
 Училище:, град/село... Утвърдил директор:.. (име, фамилия, подпис) ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 10. клас Брой учебни часове (по учебен план):
Училище:, град/село... Утвърдил директор:.. (име, фамилия, подпис) ГОДИШНО ТЕМАТИЧНО РАЗПРЕДЕЛЕНИЕ по учебния предмет химия и опазване на околната среда за 10. клас Брой учебни часове (по учебен план):
КНИГА ЗА УЧИТЕЛЯ ISBN
 КНИГА ЗА УЧИТЕЛЯ ISBN 978-954-18-1425-3 Знаци, използвани в книгата: допълнителна информация за учителя допълнителна информация за ученика любопитна информация КНИГА ЗА УЧИТЕЛЯ по химия и опазване на околната
КНИГА ЗА УЧИТЕЛЯ ISBN 978-954-18-1425-3 Знаци, използвани в книгата: допълнителна информация за учителя допълнителна информация за ученика любопитна информация КНИГА ЗА УЧИТЕЛЯ по химия и опазване на околната
Лекция Приложение на линейната многопроменлива регресия за изчисляване на топлини на образуване на алкани Дефиниция на топлина на образуване Топлина н
 Лекция Приложение на линейната многопроменлива регресия за изчисляване на топлини на образуване на алкани Дефиниция на топлина на образуване Топлина на образуване на едно химично съединение се нарича енталпията
Лекция Приложение на линейната многопроменлива регресия за изчисляване на топлини на образуване на алкани Дефиниция на топлина на образуване Топлина на образуване на едно химично съединение се нарича енталпията
Количествени задачи Задача 1. Тяло е хвърлено хоризонтално с начална скорост V0 15 m. Намерете s нормалното a n и тангенциалното a ускорение на тялото
 Количествени задачи Задача 1. Тяло е хвърлено хоризонтално с начална скорост V 15 m. Намерете нормалното a n и тангенциалното a ускорение на тялото след време t 1 от началото на движението! ( Приемете
Количествени задачи Задача 1. Тяло е хвърлено хоризонтално с начална скорост V 15 m. Намерете нормалното a n и тангенциалното a ускорение на тялото след време t 1 от началото на движението! ( Приемете
1
 Пояснения: Въпросите с номерá 1 16 се отнасят за специална част 1: Съвременни материали Въпросите с номерá 17 32 се отнасят за специална част 2: Инженерна химия 1. Равновесната степен на превръщане на
Пояснения: Въпросите с номерá 1 16 се отнасят за специална част 1: Съвременни материали Въпросите с номерá 17 32 се отнасят за специална част 2: Инженерна химия 1. Равновесната степен на превръщане на
НАРЕДБА 3 ОТ 22 МАЙ 2013 Г. ЗА ИЗИСКВАНИЯТА КЪМ ИНСТАЛАЦИИ, ПРОИЗВЕЖДАЩИ ТИТАНОВ ДИОКСИД В сила от г. Издадена от министъра на околната сре
 НАРЕДБА 3 ОТ 22 МАЙ 2013 Г. ЗА ИЗИСКВАНИЯТА КЪМ ИНСТАЛАЦИИ, ПРОИЗВЕЖДАЩИ ТИТАНОВ ДИОКСИД В сила от 04.06.2013 г. Издадена от министъра на околната среда и водите Обн. ДВ. бр.49 от 4 Юни 2013г. Глава първа.
НАРЕДБА 3 ОТ 22 МАЙ 2013 Г. ЗА ИЗИСКВАНИЯТА КЪМ ИНСТАЛАЦИИ, ПРОИЗВЕЖДАЩИ ТИТАНОВ ДИОКСИД В сила от 04.06.2013 г. Издадена от министъра на околната среда и водите Обн. ДВ. бр.49 от 4 Юни 2013г. Глава първа.
Здравейте, Това четиво е супер полезно, ако сте кандидат-студент за магистърските програми на Медицински университет-варна, независимо от предпочитана
 Здравейте, Това четиво е супер полезно, ако сте кандидат-студент за магистърските програми на Медицински университет-варна, независимо от предпочитаната от Вас специалност (медицина, дентална медицина,
Здравейте, Това четиво е супер полезно, ако сте кандидат-студент за магистърските програми на Медицински университет-варна, независимо от предпочитаната от Вас специалност (медицина, дентална медицина,
Справка за приносния характера на трудовете на д-р Стоян Иванов Гуцов
 Авторска справка за приносния характера на трудовете на доц. д-р Стоян Иванов Гуцов Изследванията на доц. д-р Стоян Иванов Гуцов са концентрирани в следните научни направления: I. Получаване и охарактеризиране
Авторска справка за приносния характера на трудовете на доц. д-р Стоян Иванов Гуцов Изследванията на доц. д-р Стоян Иванов Гуцов са концентрирани в следните научни направления: I. Получаване и охарактеризиране
Вариант 3 - ТЕСТ – всеки верен отговор по 3 точки
 Вариант - ТЕСТ всеки верен отговор по точки Топка е хвърлена вертикално нагоре По време на полета й нейното ускорение: а) нараства; б) намалява; с) остава същото; г) е нула; д) докато топката се движи
Вариант - ТЕСТ всеки верен отговор по точки Топка е хвърлена вертикално нагоре По време на полета й нейното ускорение: а) нараства; б) намалява; с) остава същото; г) е нула; д) докато топката се движи
Проект за дисертация
 СОФИЙСКИ УНИВЕРСИТЕТ СВ. КЛИМЕНТ ОХРИДСКИ ФАКУЛТЕТ ПО ХИМИЯ И ФАРМАЦИЯ КАТЕДРА ОРГАНИЧНА ХИМИЯ И ФАРМАКОГНОЗИЯ АВТОРЕФЕРАТ на дисертационен труд, представен за присъждане на образователна и научна степен
СОФИЙСКИ УНИВЕРСИТЕТ СВ. КЛИМЕНТ ОХРИДСКИ ФАКУЛТЕТ ПО ХИМИЯ И ФАРМАЦИЯ КАТЕДРА ОРГАНИЧНА ХИМИЯ И ФАРМАКОГНОЗИЯ АВТОРЕФЕРАТ на дисертационен труд, представен за присъждане на образователна и научна степен
Люсила Цанкова Емилия Лазарова Нели Гетова Георги Коцев ГЕОГРАФИЯ И ИКОНОМИКА Книга за учителя
 Люсила Цанкова Емилия Лазарова Нели Гетова Георги Коцев ГЕОГРАФИЯ И ИКОНОМИКА Книга за учителя Лиляна Боянова Красимир Николов Емилия Тодорова Ивайло Ушагелов ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА Книга за
Люсила Цанкова Емилия Лазарова Нели Гетова Георги Коцев ГЕОГРАФИЯ И ИКОНОМИКА Книга за учителя Лиляна Боянова Красимир Николов Емилия Тодорова Ивайло Ушагелов ХИМИЯ И ОПАЗВАНЕ НА ОКОЛНАТА СРЕДА Книга за
Microsoft Word - tema_7_klas_2009.doc
 РЕГИОНАЛЕН ИНПЕКТОРАТ ПО ОБРАЗОАНИЕТО, ОФИЯ-ГРАД Национално състезание-тест по математика за VІІ клас Общински кръг, офия, февруари 009 г. Утвърдил:... аня Кастрева началник РИО, офия-град Тестът съдържа
РЕГИОНАЛЕН ИНПЕКТОРАТ ПО ОБРАЗОАНИЕТО, ОФИЯ-ГРАД Национално състезание-тест по математика за VІІ клас Общински кръг, офия, февруари 009 г. Утвърдил:... аня Кастрева началник РИО, офия-град Тестът съдържа
НАУЧНИ ТРУДОВЕ НА РУСЕНСКИЯ УНИВЕРСИТЕТ , том 48, серия 10 Кинетика на преориентация на F A центрове, при осветяване с неполяризирана F A светли
 Кинетика на преориентация на F центрове, при осветяване с неполяризирана F светлина Димитър Попов, Йордан Димов Reorienaion Kineics Of F Ceners In KCL:Na Obained Under Illuminaion Wih Unpolarized F Lighs:
Кинетика на преориентация на F центрове, при осветяване с неполяризирана F светлина Димитър Попов, Йордан Димов Reorienaion Kineics Of F Ceners In KCL:Na Obained Under Illuminaion Wih Unpolarized F Lighs:
1 Термодинамика на идеалния газ: между молекулите няма взаимодействие. Изотермичното свиване нe води до промяна на вътрешната енергия. RT pv E E U R c
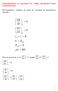 Термодинамика на идеалния газ: между молекулите няма взаимодействие. Изотермичното свиване нe води до промяна на вътрешната енергия. E E ot kin 0 0 0 Нека да докажем, че от 0 следва: 0, 0, 0 0 0 ) ( )
Термодинамика на идеалния газ: между молекулите няма взаимодействие. Изотермичното свиване нe води до промяна на вътрешната енергия. E E ot kin 0 0 0 Нека да докажем, че от 0 следва: 0, 0, 0 0 0 ) ( )
PowerPoint-Präsentation
 Полимерен комплекс с радиационно-защитни свойства Виолета Митова, Кольо Троев Институт по полимери - БАН Основни проблеми в хуманната медицина - странични ефекти на лекарствените вещества върху нормалните
Полимерен комплекс с радиационно-защитни свойства Виолета Митова, Кольо Троев Институт по полимери - БАН Основни проблеми в хуманната медицина - странични ефекти на лекарствените вещества върху нормалните
IMH'I'AS'Lecture'ALL'UCII'r'19
 ИНСТРУМЕНТАЛНИ МЕТОДИ ЗА АНАЛИЗ АТОМНА СПЕКТРОХИМИЯ ЛЕКЦИЯ 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ СПЕКТРИ Химия ІІ курс редовно, летен семестър 2019 Pag Лекция 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ
ИНСТРУМЕНТАЛНИ МЕТОДИ ЗА АНАЛИЗ АТОМНА СПЕКТРОХИМИЯ ЛЕКЦИЯ 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ СПЕКТРИ Химия ІІ курс редовно, летен семестър 2019 Pag Лекция 2 КВАНТОВА ПРИРОДА НА МИКРОСВЕТА. АТОМНИ
Лекция 6
 Лекция 8 Радиационен топлообмен Основни положения Радиационният способ на пренасяне на топлинна енергия се характеризира с това, че енергията се пренася посредством електромагнитни вълни. Пренасянето на
Лекция 8 Радиационен топлообмен Основни положения Радиационният способ на пренасяне на топлинна енергия се характеризира с това, че енергията се пренася посредством електромагнитни вълни. Пренасянето на
19 29 юли 2018 Братислава, СЛОВАКИЯ Прага, ЧЕШКА РЕПУБЛИКА ТЕОРЕТИЧНИ ЗАДАЧИ Country: Bulgaria Name as in passport: Student code: Langua
 19 29 юли 2018 Братислава, СЛОВАКИЯ Прага, ЧЕШКА РЕПУБЛИКА www.50icho.eu ТЕОРЕТИЧНИ ЗАДАЧИ Country: Bulgaria Name as in passport: Student code: Language: Bulgarian УСПЕХ!!! 50 МОХ 2018 Международна Олимпиада
19 29 юли 2018 Братислава, СЛОВАКИЯ Прага, ЧЕШКА РЕПУБЛИКА www.50icho.eu ТЕОРЕТИЧНИ ЗАДАЧИ Country: Bulgaria Name as in passport: Student code: Language: Bulgarian УСПЕХ!!! 50 МОХ 2018 Международна Олимпиада
Basfoliar Cereals SL
 Green Game LTD 2018 Продуктова гама Чиста технология ( 3,4-dimethylpyrazole phosphate - DMPP Nitrification Inhibitor ) Чиста технология Инхибитор на нитрификация (DMPP) BASF/COMPO Развитие (1994-1999 )
Green Game LTD 2018 Продуктова гама Чиста технология ( 3,4-dimethylpyrazole phosphate - DMPP Nitrification Inhibitor ) Чиста технология Инхибитор на нитрификация (DMPP) BASF/COMPO Развитие (1994-1999 )
Microsoft Word - TAB_5.doc
 Таблица 5: Граници на годишното постъпване на отделни радионуклиди в организма на персонала чрез вдишване (ГГП ИНХ ) или поглъщане (ГГП ПО ) и граница на средногодишната обемна активност (ГСГОА В ) на
Таблица 5: Граници на годишното постъпване на отделни радионуклиди в организма на персонала чрез вдишване (ГГП ИНХ ) или поглъщане (ГГП ПО ) и граница на средногодишната обемна активност (ГСГОА В ) на
Приложение на методите на Рунге Кута за решаване на уравненията за отравяне на ядрения реактор 1. Въведение В доклада са направени поредица от изчисле
 Приложение на методите на Рунге Кута за решаване на уравненията за отравяне на ядрения реактор 1. Въведение В доклада са направени поредица от изчисления върху уравненията за отравяне на ядрения реактор
Приложение на методите на Рунге Кута за решаване на уравненията за отравяне на ядрения реактор 1. Въведение В доклада са направени поредица от изчисления върху уравненията за отравяне на ядрения реактор
НАРЕДБА № 3 ОТ 1 АВГУСТ 2008 Г. ЗА НОРМИТЕ ЗА ДОПУСТИМО СЪДЪРЖАНИЕ НА ВРЕДНИ ВЕЩЕСТВА В ПОЧВИТЕ
 НАРЕДБА 3 ОТ 1 АВГУСТ 2008 Г. ЗА НОРМИТЕ ЗА ДОПУСТИМО СЪДЪРЖАНИЕ НА ВРЕДНИ ВЕЩЕСТВА В ПОЧВИТЕ В сила от 12.08.2008 г. Издадена от Министерството на околната среда и водите, Министерството на здравеопазването
НАРЕДБА 3 ОТ 1 АВГУСТ 2008 Г. ЗА НОРМИТЕ ЗА ДОПУСТИМО СЪДЪРЖАНИЕ НА ВРЕДНИ ВЕЩЕСТВА В ПОЧВИТЕ В сила от 12.08.2008 г. Издадена от Министерството на околната среда и водите, Министерството на здравеопазването
